Bagaimana menamai senyawa kimia
Pengarang:
Laura McKinney
Tanggal Pembuatan:
2 April 2021
Tanggal Pembaruan:
26 Juni 2024

Isi
- tahap
- Metode 1 dari 3: Nomenklatur senyawa ionik
- Metode 2 dari 3: Nomenklatur senyawa poliatomik
- Metode 3 dari 3: Nomenklatur Senyawa Kovalen
Berhasil di bidang kimia membutuhkan pengetahuan bagaimana menamai senyawa kimia dasar. Panduan ini memberi Anda aturan dasar tentang proses penamaan untuk senyawa kimia dan cara menetapkan nama untuk senyawa yang tidak Anda kenal.
tahap
Metode 1 dari 3: Nomenklatur senyawa ionik
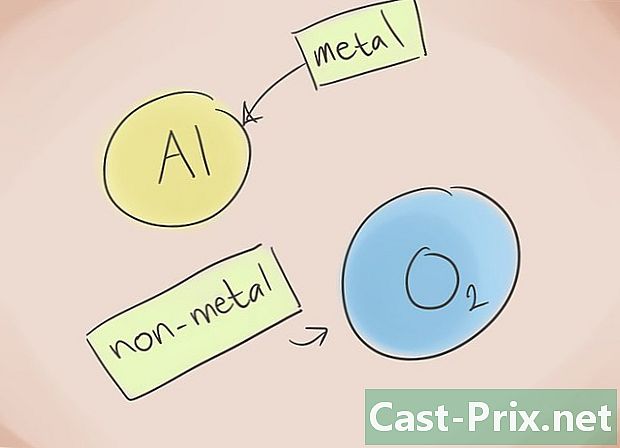
- Apa itu senyawa ionik? Senyawa ionik terdiri dari logam dan non-logam. Kemudian lihat Tabel Unsur Berkala untuk mengetahui kategori mana yang termasuk dalam unsur yang ada dalam senyawa.
-

Bentuk namanya. Tidak ada yang lebih mudah daripada menamai senyawa ionik dari dua elemen. Memang, bagian pertama dari nama senyawa sesuai dengan nama elemen non-logam bertuliskan "ure" akhiran sedangkan yang kedua sesuai dengan nama elemen logam. Ada pengecualian: oksida, fosfida, nitrida, sulfida.- Contoh: Al2O3. al2 = Aluminium; O3 = Oksigen. Jadi nama senyawa tersebut adalah "aluminium oksida".
-
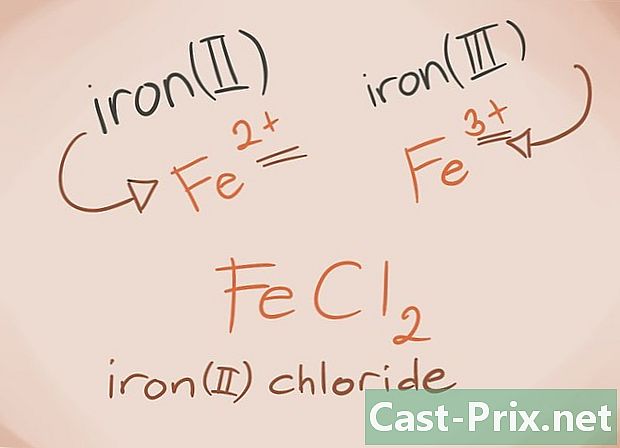
Ketahui logam transisi Logam transisi adalah logam yang ditemukan di blok D dan F pada tabel periodik. Atas nama senyawa, muatan pada logam-logam ini ditulis dalam angka Romawi. Ini karena logam transisi dapat membawa lebih banyak muatan dan membentuk lebih banyak senyawa.- Contoh: FeCl2 dan FeCl3. Fe = Besi; Cl2 = -2 Klorida; Cl3 = Klorida -3. Seperti namanya, akan ada besi klorida (II) dan besi klorida (III).
Metode 2 dari 3: Nomenklatur senyawa poliatomik
-

Anda perlu memahami apa senyawa poliatomik itu. Senyawa poliatomik adalah senyawa yang dibentuk oleh sekelompok datoma yang terkait satu sama lain; seluruh kelompok yang membawa muatan positif atau negatif. Kemudian ada tiga tindakan dasar yang dapat Anda lakukan pada senyawa poliatomik:- Anda dapat menambahkan hidrogen ke bagian pertama dari senyawa. Kata "hidrogen" memang ditambahkan di awal nama senyawa. Ini akan mengurangi nilai muatan negatif satu per satu. Misalnya, "karbonat" CO3 menjadi HCO "hidrogen karbonat"3.

- Anda juga dapat menghilangkan oksigen dari senyawa. Beban tidak berubah, tetapi akhiran "-ate" dari senyawa diubah menjadi "-ique". Misalnya transformasi dari: TIDAK3 dalam NO2 kita beralih dari nitrat ke nitrat. "

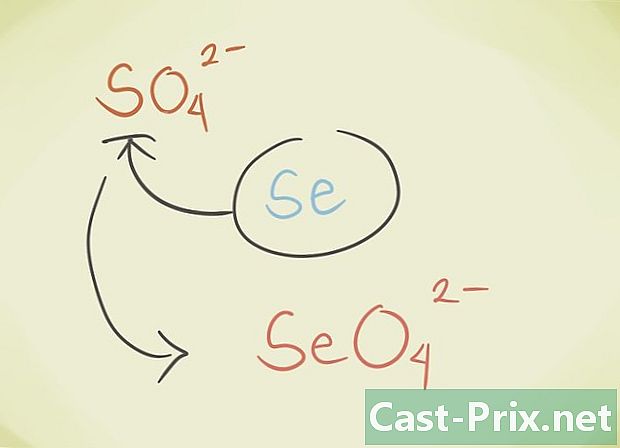
- Anda dapat mengganti latom tengah senyawa dengan atom lain yang termasuk dalam kelompok periodik yang sama. Misalnya, SO sulfat4 dapat digantikan oleh Selenate SeO4.
- Anda dapat menambahkan hidrogen ke bagian pertama dari senyawa. Kata "hidrogen" memang ditambahkan di awal nama senyawa. Ini akan mengurangi nilai muatan negatif satu per satu. Misalnya, "karbonat" CO3 menjadi HCO "hidrogen karbonat"3.
-

Hafalkan kelompok dion yang paling umum. Kelompok-kelompok di bawah ini digunakan untuk membentuk sebagian besar senyawa poliatomik. Mengikuti peningkatan urutan muatan negatifnya, kami memiliki:- ion hidroksida: OH
- ion nitrat: TIDAK3
- Ion hidrogen karbonat: HCO3
- ion permanganat: MnO4
- ion karbonat: CO3
- ion kromat: CrO4
- ion dikromat: Cr2O7
- ion sulfat: JADI4
- ion sulfit: JADI3
- ion tiosulfat: S2O3
- Ion fosfat: PO4
- ion amonium: NH4
- Bentuk nama majemuk dari daftar di atas. Bentuk asosiasi nama dengan salah satu item yang terkait dengan grup. Jika elemen ditempatkan sebelum gugus ionik, maka nama elemen hanya akan ditambahkan ke awal nama senyawa.
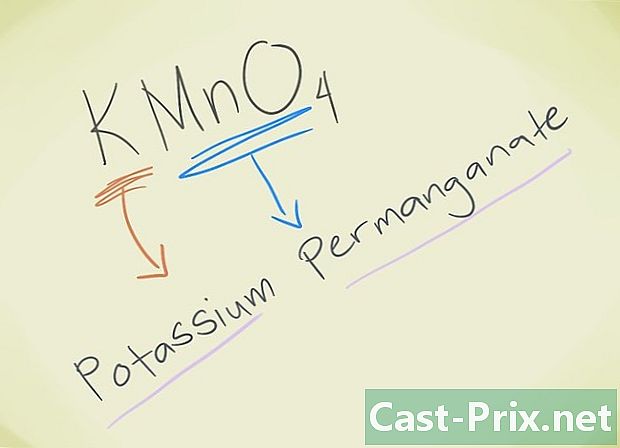
- Contoh: KMnO4. Anda harus dapat mengetahui bahwa singa MnO4 sesuai dengan singa permanganat. K mengacu pada kalium. Jadi senyawa Anda akan disebut Permanganate Potassium.
- Contoh: NaOH. Anda mungkin akan mengerti di sini bahwa itu OHOH. Na adalah, natrium, jadi senyawa itu akan disebut natrium hidroksida.

- Contoh: KMnO4. Anda harus dapat mengetahui bahwa singa MnO4 sesuai dengan singa permanganat. K mengacu pada kalium. Jadi senyawa Anda akan disebut Permanganate Potassium.
Metode 3 dari 3: Nomenklatur Senyawa Kovalen
-
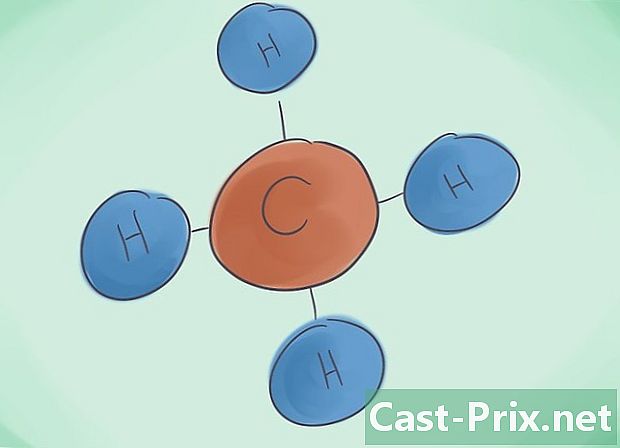
Apa itu senyawa kovalen? Senyawa kovalen dihasilkan dari asosiasi setidaknya dua elemen non-logam. Nama senyawa ditentukan oleh jumlah datoma yang menyusunnya. Awalan bahasa Yunani di sebelah nama ini menunjukkan jumlah molekul yang ada dalam senyawa. -
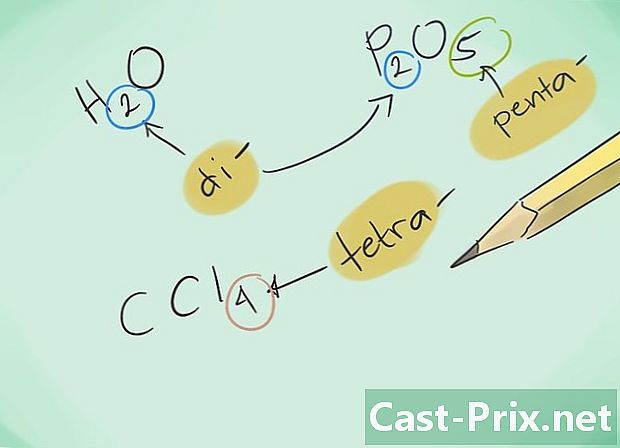
Biasakan diri Anda dengan awalan. Hafalkan awalan berikut untuk senyawa dari 1 hingga 8 atom:- 1 atom - "Mono-"
- 2 atom - "Di-"
- 3 atom - "Tri-"
- 4 atom - "Tetra-"
- 5 atom - "Penta-"
- 6 atom - "Hexa-"
- 7 atom - "Hepta-"
- 8 atom - "Okta-"
- Kemudian beri nama senyawa. Beri nama senyawa yang dihasilkan menggunakan awalan yang sesuai. Awalan harus dicangkokkan pada setiap elemen yang membentuk senyawa dengan beberapa atom.
- Contoh: CO akan kembali ke karbon monoksida sedangkan CO2 akan menunjuk karbon dioksida.
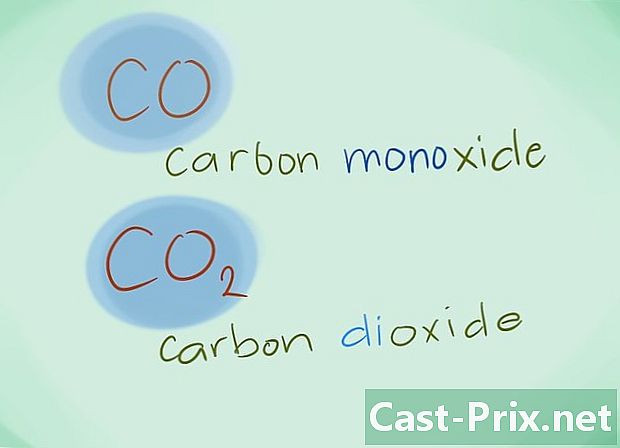
- Contoh: N2S3 akan sesuai dengan nitrous trisulfide.

- Dalam kebanyakan kasus, awalan "mono" dapat dihilangkan; ini, lebih dari kurangnya awalan, menginduksi bahwa yang terakhir harus digunakan. Awalan ini terus digunakan dalam kasus karbon monoksida mengingat fakta bahwa penggunaan ini kembali ke kilau pertama kimia.
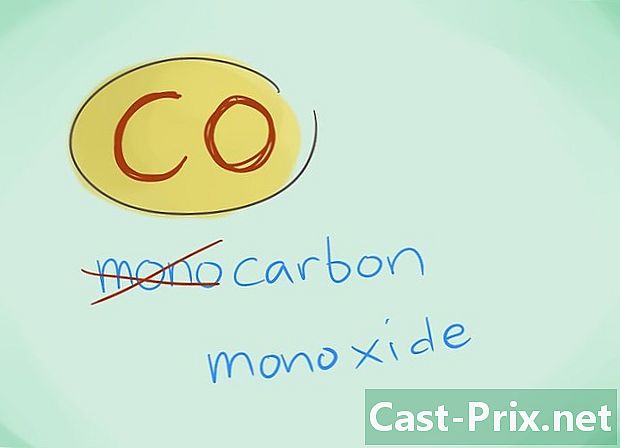
- Contoh: CO akan kembali ke karbon monoksida sedangkan CO2 akan menunjuk karbon dioksida.
- Tentu saja, Anda mencurigai bahwa beberapa pengecualian berlaku untuk semua aturan ini; tahan misalnya, rumus ini, CaCl2Anda berharap melihatnya "kalsium diklorida," yang TIDAK. Senyawa Anda hanya akan menyimpan nama kalsium klorida.
- Perlu juga dicatat bahwa semua ini tidak berlaku untuk kimia organik.
- Aturan rinci di sini dimaksudkan untuk audiens pemula dalam kimia dan sains. Ada aturan yang sangat berbeda ketika Anda melewati tahap kimia lanjut, seperti aturan tentang valensi variabel.